In den EU-Ländern sind bislang vier Impfstoffe gegen das Corona-Virus zugelassen. Nun könnte zwei weitere folgen. Die unterscheiden sich aber in einem entscheidenden Punkt von seinen Vorgängern.
Neue Totimpfstoffe gegen COVID-19
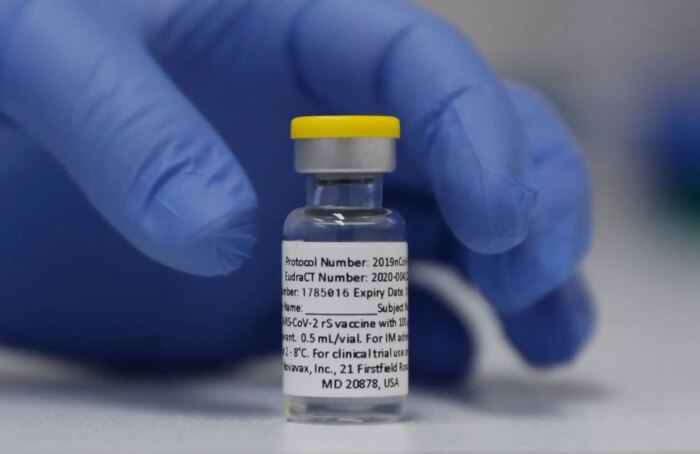
In Deutschland sind bislang zwei mRNA-Impfstoffe und zwei Vektorimpfstoffe zugelassen. Damit basierte die Impfkampagne bisher auf Technologien, die noch nie zuvor eingesetzt wurden.
<div class=“manual-ad“></div>
Doch nun ziehen die altbekannten Vakzine nach: Mit dem US-amerikanischen Novavax und dem indischen Covaxin dürften es bald auch zwei Totimpfstoffe in Deutschland zur Zulassung bringen.
In einer gerade im medizinischen Fachjournal „The Lancet“ veröffentlichten Phase-3-Studie erzielte das Präparat Covaxin eine Wirksamkeit von knapp 80 Prozent. Novavax erreichte sogar eine 90-prozentige Schutzwirkung, berichtet die Studie, die im „New England Journal of Medicine“ veröffentlicht wurde, berichtet „Health News“.
<div class=“manual-ad“></div>
Bei beiden neuen Impfstoffen handelt es sich beide um sogenannte Totimpfstoffe. Das bedeutet, sie verwenden inaktivierte Vollviren, die nicht replikationsfähig sind, um im Körper eine Immunreaktion hervorzurufen. Nach diesem Prinzip funktionieren etwa auch die bisher eingesetzten Impfstoffe gegen Influenza, Tetanus und HPV.
Der Impfstoff von Novavax setzt allerdings zusätzlich einen Wirkverstärker ein, der aus dem chilenischen Seifenrindenbaum gewonnen wird. In Indonesien ist der Impfstoff bereits zugelassen, in diversen weiteren Ländern laufen zurzeit Zulassungsverfahren.
<div class=“manual-ad“></div>
Für das Präparat Covaxin gab die Weltgesundheitsorganisation (WHO) kürzlich eine Empfehlung für den Notfalleinsatz für Personen ab 18 Jahren heraus. Sowohl für diese als auch für die Novavax-Impfung werden zwei Dosen verabreicht im Abstand von drei (Novavax) beziehungsweise vier Wochen (Covaxin).
Einfache Lagerung und weniger Skepsis
Klarer Vorteil der beiden neuen Wirkstoffe ist die Lagerung: Sie können bei normaler Kühlschranktemperatur gelagert und transportiert werden. Das erleichtert den Einsatz der Impfstoffe in weniger wohlhabenden Ländern.
Auch hierzulande sollten die neuen Totimpfstoffe einen wichtigen Dienst leisten schaffen: Viele Menschen, die sich bisher aus Skepsis gegenüber den neuartigen Funktionsweisen der COVID-19-Impfstoffe nicht haben impfen lassen, stehen den Totimpfstoffen offener gegenüber.
<div class=“manual-ad“></div>
Novavax
Der US-Hersteller Novavax hat für seinen Corona-Impfstoff eine Marktzulassung in der EU beantragt. Das teilte die zuständige europäische Arzneimittelbehörde EMA am Mittwoch in Amsterdam mit.
Ein Expertenteam werde nun die Daten des Herstellers prüfen und Risiken gegen Nutzen abwägen. Eine Entscheidung wird in einigen Wochen erwartet, wie die EMA mitteilte.
Die Experten hatten bereits im laufenden Prüfverfahren Studien zur Wirkung bewertet. Auch sei eine vorläufige Prüfung von möglichen Risiken bereits abgeschlossen worden. Sollte die EMA eine bedingte Marktzulassung empfehlen, muss die EU-Kommission noch endgültig zustimmen. Das aber gilt als Formsache. Bisher sind in der EU vier Impfstoffe zugelassen worden.
<div class=“manual-ad“></div>
Das Novavax-Produkt namens Nuvaxovid (NVX-CoV2373) ist im Gegensatz zu den bisher zugelassenen Impfstoffen weder ein mRNA-Impfstoff – wie die Präparate von Biontech und Moderna – noch ein Vektor-Impfstoff wie die von Astrazeneca und Johnson & Johnson: Das Vakzin enthält winzige Partikel, die aus einer im Labor hergestellten Version des Spike-Proteins von Sars-CoV-2 bestehen. Wie alle Impfstoffe soll Nuvaxovid das Immunsystem auf eine mögliche Infektion vorbereiten.
Quellen, DPA, Health News
<a href=“//clk.tradedoubler.com/click?p=272689&a=3132394&g=24440756″ target=“_blank“>
</a>